Введите слово или словосочетание на любом языке 👆
Язык:
Перевод и анализ слов искусственным интеллектом ChatGPT
На этой странице Вы можете получить подробный анализ слова или словосочетания, произведенный с помощью лучшей на сегодняшний день технологии искусственного интеллекта:
- как употребляется слово
- частота употребления
- используется оно чаще в устной или письменной речи
- варианты перевода слова
- примеры употребления (несколько фраз с переводом)
- этимология
Что (кто) такое Фосфаты - определение
Фосфат; Ортофосфаты; Метафосфат; Гидроортофосфат; Дигидроортофосфат; Дигидрофосфат
Найдено результатов: 34
ФОСФАТЫ
соли и эфиры фосфорных кислот. Различают: ортофосфаты (соли и эфиры ортофосфорной кислоты Н3РО4) и полимерные фосфаты (полифосфаты, метафосфаты, ультрафосфаты). Соли входят в состав фосфорных удобрений, минеральных подкормок, моющих средств и др. Эфиры - экстрагенты, гидравлические и смазочные жидкости, пластификаторы, антипирены и др.
ФОСФАТЫ
соли или эфиры фосфорных кислот.
фосфаты
мн.
Соли фосфорной кислоты, применяемые как удобрение и моющие средства, а также в пищевой промышленности.
Соли фосфорной кислоты, применяемые как удобрение и моющие средства, а также в пищевой промышленности.
Фосфаты
соли и эфиры фосфорных кислот. Из солей различают ортофосфаты и полимерные (или конденсированные) Ф. Последние делят на полифосфаты, имеющие линейное строение фосфат-анионов, метафосфаты с кольцеобразным (циклическим) фосфат-анионом и ультрафосфаты с сетчатой, разветвленной структурой фосфат-аниона. К Ф. относят также весьма стойкие соединения - фосфаты бора BPO4 и алюминия AlPO4 (хотя правильнее было бы считать их смешанными ангидридами P2O5 и B2O3; P2O5 и Al2O3).
Ортофосфаты - соли ортофосфорной кислоты H3PO4 - известны одно-, двух- и трёхзамещённые. Однозамещённые ортофосфаты, содержащие анион H2PO4, растворимы в воде, из двух- и трёхзамещённых ортофосфатов, содержащих соответственно анионы HPO42- и PO43-, растворимы только соли щелочных металлов и аммония. Трёхзамещённые ортофосфаты, за исключением триаммоний фосфата (NH4)3PO4․3H2O, термически устойчивы; трикальцийфосфат заметно диссоциирует лишь при температурах выше 2000 °С (диссоциация улучшается под вакуумом): Ca3(PO4)2 = 3CaO + P2O5. При нагревании одно- и двухзамещённых ортофосфатов происходит их дегидратация с выделением структурной воды и образованием полимерных (линейных или кольцевых) фосфатов по схеме:
(n-2) MeH2PO4 (2Me2HPO4 (Men + 2PnO3n + 1 + (n-1) H2O
(где n - степень полимеризации).
Все встречающиеся в природе соединения фосфора представляют собой ортофосфаты (см. Фосфаты природные). В промышленности растворимые в воде ортофосфаты получают по следующей схеме: 1) производство из природных Ф. (главным образом апатитов (См. Апатиты)) ортофосфорной кислоты (см. Фосфорные кислоты); 2) взаимодействие ортофосфорной кислоты с гидроокисями, аммиаком, хлоридами или карбонатами, например:
H3PO4 + MH3 = NH4H2PO4
H3PO4 + KCl = KH2PO4 - HCl
Труднорастворимые ортофосфаты тяжелых металлов (например, Ag, Cu) образуются в результате обменных реакций, например:
2Na2HPO4 + 3AgNO3 = Ag3PO4 + 3NaNO3 + NaH2PO4
Полимерные Ф. различных структурных типов могут быть описаны формулами: линейные полифосфаты Men + 2PnO3n + 1, или
кольцевые метафосфаты MenPnO3n, или
(где n - степень полимеризации).
Свойства полимерных Ф. зависят от характера катиона, строения фосфат-аниона, степени полимеризации, структуры фосфата и др. Так, например, растворимость линейных полифосфатов, как правило, падает с увеличением степени полимеризации, но может быть увеличена путём модифицирования полифосфатов, например изменением скорости охлаждения расплава.
Получают полимерные Ф. (линейные и кольцевые) в основном термической дегидратацией одно- и двухзамещённых ортофосфатов или нейтрализацией соответствующих поли- или мета- (циклических) фосфорных кислот:
Hn + 2PnO3n + 1 + nNH3 = (NH4) n H2PnO3n + 1
(иногда эти процессы совмещаются, как, например, при высокотемпературной аммонизации ортофосфорной кислоты для получения полифосфатов аммония). В промышленных масштабах эти способы используют для получения пиро-, триполифосфатов натрия (соответственно Na4P2O7, Na5P3O10) и в меньшей степени - калия, а также полимерных метафосфатов (натрий-фосфатные стекла, метафосфат калия и др.).
Из циклических метафосфатов наиболее изучены тримета-, тетрамета-, гексамета- и октаметафосфаты.
Ультрафосфаты - соединения общей формулы MenRPnOn (5 + R)/2, где R = Me2O/P2O5, как правило, аморфные, стеклообразные вещества, гигроскопичные, легко гидролизующиеся на воздухе с образованием поли- и метафосфатов. Последние в присутствии большого количества воды могут гидролизоваться за счёт полного расщепления Р-О-Р-связей вплоть до ортофосфатов. Выделенные в кристаллическом виде ультрафосфаты кальция, магния, марганца и некоторых лантаноидов, как правило, не гигроскопичны. Ультрафосфаты образуются в результате термической дегидратации смеси ортофосфатов с фосфорными кислотами или с фосфорным ангидридом, т. е. при наличии условия
О < Me2O/P2O5 < 1.
Ф. кальция, аммония, калия и др. широко применяются в качестве фосфорных удобрений (См. Фосфорные удобрения). В 70-е гг. 20 в. выросло производство кормовых фосфатов [например, обесфторенные Ф., Преципитат, динатрийфосфат, фосфаты мочевины - H3PO4․(NH2)2CO и др.]. Ф. натрия и калия (особенно триполифосфаты) применяют в качестве компонентов жидких и порошкообразных моющих средств (См. Моющие средства) и поверхностно-активных веществ (См. Поверхностно-активные вещества) при буровых работах, в цементной, текстильной промышленности при подготовке шерсти, хлопка к белению и крашению. Ф. используют в пищевой промышленности в качестве рыхлителей теста, например (NH4)2HPO4. Некотоpые Ф. (например, BPO4) применяют в качестве катализаторов (См. Катализаторы) в реакциях органического синтеза. Ф. преимущественно щелочных металлов входят в состав эмалей, глазурей, стекол, огнестойких материалов (как Антипирены), а также мягких абразивов; они используются при фосфатировании (См. Фосфатирование) металлов (Mg, Fe, Zn). Кристаллы однозамещённых фосфатов калия, аммония применяются как Сегнетоэлектрики и Пьезоэлектрические материалы. Ф. используются в фармацевтической промышленности при изготовлении лекарственных препаратов (например, фосфакол, АТФ - аденозинтрифосфат и др.), зубных паст и порошков.
Л. В. Кубасова.
Из эфиров фосфорных кислот наиболее известны одно-, двух- и трёхзамещённые ортофосфаты, соответственно ROP (O)(OH)2, (RO)2P (O) OH и (KO)3PO (где R - алкил, арил или гетероциклический остаток). Получаются при взаимодействии POCl3 со спиртами:
POCl3 + 3ROH → (RO)3PO
POCl3 + 2ROH → (RO)2P (O) Cl 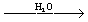 (RO)2P (O) OH
(RO)2P (O) OH
и др. способами.
Применяются как Пестициды, Присадки к маслам, экстрагенты и т.д. Некоторые органические Ф. (Нуклеиновые кислоты, Аденозинфосфорные кислоты) выполняют важные функции в живых организмах.
Э. Е. Нифантьев.
Лит.: Продан Е. А., Продан Л. И., Ермоленко Н. Ф., Триполифосфаты и их применение, Минск, 1969; см. также лит. при ст. Фосфор.
Фосфаты.
Фосфаты
Фосфа́ты — соли фосфорных кислот, например ортофосфат калия K3PO4. Различают ортофосфаты и конденсированные фосфаты, содержащие более одного атома P, образующие связи P—O—P.
ФОСФАТ
а, м. хим.
Соль фосфорной кислоты, применяемая как удобрение (ср. суперфосфат) и моющее средство, а также используемая в пищевой промышленности.
фосфат
м.
см. фосфаты.
см. фосфаты.
фосфат
общее название солей и эфиров фосфорной кислоты.
фосфат
1. Соль фосфорной кислоты, применяемая в технике, медицине и (как составная часть удобрения) в агрономии (·хим. ). Фосфат кальция. Фосфат алюминия.
2. Минерал, содержащий фосфорную кислоту (минер.).
Натрия фосфаты
натриевые соли фосфорных кислот, например Na3PO4; см. Фосфаты, Фосфаты натрия.
Википедия
Фосфаты

Фосфа́ты — соли фосфорных кислот, например ортофосфат калия K3PO4. Различают ортофосфаты и конденсированные фосфаты, содержащие более одного атома P, образующие связи P—O—P.



